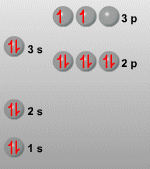
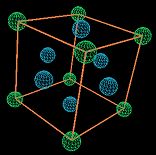
Es un
elemento muy abundante en la naturaleza, ocupa el segundo lugar en
esta faceta en la corteza terrestre, más de la cuarta parte. El
primero es el oxígeno. En su forma amorfa se presenta como polvo
parduzco. En la cristalina, su color es grisáceo, azulado. La
primera es más activa. El cristal es muy duro (raya el vidrio), poco soluble y
brillo metalizado.
Es importantísimo, debido a su
caracter semiconductor, en la industria informática ya que es
necesario para la fabricación de chips y transistores. También es
utilizado en la fabricación de cementos y ladrillo.
Resiste la
acción de la mayoría de los ácidos, reacciona con los halógenos y
las bases diluidas. Es relativamente inerte. |